中文摘要
目的 开发抗NF-κB受体激活蛋白配体(receptor activator of NF-κB ligand,RANKL)单克隆抗体(单抗)的纯化工艺。
方法 采用深层过滤澄清上游细胞培养液去除细胞,澄清后的培养液经过亲和层析捕获、低pH病毒灭活、阴离子交换层析、阳离子交换层析、除病毒过滤、超滤浓缩、透析置换、除菌过滤等步骤,获得单抗原液。通过收率和产品相关杂质去除情况评价亲和层析纯化效果,通过监测穿透点计算填料的动态载量(dynamic binding capacity,DBC);通过考察不同的pH和温度条件对样品的纯度和活性影响,确定低pH病毒灭活条件;通过考察目的蛋白在不同缓冲体系下的稳定性、工艺相关杂质去除情况,确定合适的阴离子交换层析缓冲体系并考察纯化效果和DBC;通过线性洗脱,分段收集考察杂质情况确定阳离子交换层析工艺参数;通过处理量、通量、流量衰减确定病毒滤器的型号;根据浓缩、透析及过滤除菌说明书和平台技术确定滤膜孔径、进液流速和跨膜压力,再根据确定的参数进行浓缩及透析置换;最后经0.2 μm膜除菌过滤获得原液,并检测纯度和杂质。
结果 以MabSelect SuRe为亲和层析填料,DBC 45.3 mg/mL填料,25 mmol/L 三羟甲基氨基甲烷(Tris)-盐酸(pH7.5)为平衡液,150 mmol/L醋酸(pH2.8)为洗脱液;pH3.5灭活1 h;以Sepharose QFF为阴离子填料,最大DBC 60 mg/mL填料,50 mmol/L Tris-醋酸(pH7.5)为平衡液;SP HP为阳离子填料,上样量21.9 mg/mL,100%缓冲液A(10 mmol/L柠檬酸,pH5.5)—100%缓冲液B(10 mmol/L柠檬酸+1 mol/L NaCl,pH5.5)线性洗脱20柱体积;以Viresolve Pro为除病毒过滤器;采用PLCTK 30 kDa超滤膜包(C流道)超滤透析浓缩至(40.00±5.00) mg/mL,并以等体积方式10倍体积置换成原液缓冲液后除菌过滤;单抗纯度和杂质含量均符合质量标准。
结论 成功开发出抗RANKL单抗的纯化工艺,产品符合要求。

扫码获取原文PDF

正文
单克隆抗体(单抗)药物因其高特异性和靶向性,已成为治疗肿瘤、自身免疫性疾病和感染性疾病的重要工具。随着生物技术的快速发展,抗体药物的研发与生产日益受到关注,纯化工艺作为抗体生产的关键环节,直接影响产品的质量、安全性和生产效率。抗NF-κB受体激活蛋白(receptor activator of NF-κB,RANK)配体(RANK ligand,RANKL)单抗通过抑制RANKL与RANK的结合,阻断破骨细胞的活化和分化,在骨质疏松症和骨相关疾病的治疗中临床效果显著。
抗RANKL抗体的复杂结构和功能特性对其纯化工艺提出了更高的要求,如何高效去除宿主细胞蛋白(host cell protein,HCP)、核酸、聚体及病毒等杂质,同时保持抗体的活性和稳定性,是工艺开发中的核心挑战。目前,单抗的纯化通常采用多步层析技术,包括亲和层析、离子交换层析和疏水相互作用层析等。尽管已有多种平台化工艺可供参考,但特定抗体的纯化仍需根据其理化性质和杂质谱进行个性化优化。
本研究旨在开发高效、稳定的抗RANKL单抗纯化工艺,通过系统优化各步骤的关键参数,包括亲和层析填料的选择、低pH灭活条件的确定、离子交换层析缓冲体系的筛选以及除病毒过滤器的性能评估等,最终获得符合质量要求的抗体原液。研究不仅可为抗RANKL抗体的生产提供可靠的技术路线,也可为其他单抗的纯化工艺开发提供借鉴,为抗体药物的工业化生产和临床应用奠定基础。
1
材料与方法
1.1
材料
抗RANKL单抗(R抗体)基因由珠海市丽珠单抗生物技术有限公司自主设计并构建,通过基因工程将目的基因转染至中国仓鼠卵巢细胞,经过克隆筛选后获得单克隆细胞培养表达,收取细胞培养液。
三羟甲基氨基甲烷(Tris)、三水醋酸钠、冰醋酸、氢氧化钠、氯化钠均购自美国J.T.Baker公司,均为分析纯;分析纯山梨醇购自德国默克公司;注射级聚山梨酯20购自法国Seppic公司;对照药Prolia(原研药)购自美国Amgen公司。
亲和层析填料MabSelect SuRe〔柱体积(column volume,CV)1.0 mL〕、MabSelect SuRe LX(CV 4.7 mL)均购自美国GE公司,Minichrom Column Eshmuno A(CV 5.0 mL)购自美国Merck公司,Amsphere Protein A Column JWT 203CE(CV 5.0 mL)购自日本JSR Life Sciences公司。阴离子交换层析填料Sepharose Q FF(CV 4.7 mL)和阳离子交换层析填料SP HP(CV 1.0 mL)均购自美国GE公司。
除病毒滤器信息见表1。PLCTK 30 kDa系列超滤膜包(C型流道,复合再生纤维素材质,截留孔径30 kDa),购自美国Millipore公司,货号P3C030C05,面积0.5 m2,上样载量为240~360 g/m2。Sartopore 2系列除菌滤器(聚醚砜材质,孔径0.45 μm+0.2 μm),购自德国赛多利斯公司,货号5445307H7--SS--A,面积500 cm2,上样载量<206 L/m2。

1.2
亲和层析工艺开发
分别用市场上4款耐碱亲和层析填料(1.1节)进行亲和层析,比较填料的动态载量(dynamic binding capacity,DBC)和纯化效果。
1.2.1 DBC的测定和比较 以相同保留时间(6 min)用4款填料分别上样,设定穿透点(流穿液中目的物浓度达到进样浓度一定比例时)约为5%,计算公式:DBC=(上样蛋白总量-穿透点前流出蛋白总量)/CV。
1.2.2 纯化效果的比较 分别使用不同填料,按70% DBC上样R抗体进行亲和层析,比较纯化效果。考察以下指标:收率=收集液中蛋白总量/上样蛋白总量;产品相关杂质(聚体和降解片段)通过分子排阻色谱-高效液相色谱(size exclusion chromatography-high performance liquid chromato-graphy,SEC-HPLC)、非还原十二烷基硫酸钠毛细管电泳(non-reduced capillary electrophoresis sodium dodecyl sulfate,nrCE-SDS)、成像毛细管等电聚焦电泳(imaged capillary isoelectric focusing,icIEF)检测;工艺相关杂质(HCP、脱落的亲和层析填料配基蛋白质A)通过ELISA检测;宿主DNA通过实时荧光定量PCR检测。
按下面步骤进行层析。用25 mmol/L Tris-盐酸(pH7.5)平衡1个CV;以保留时间6 min上样;依次用25 mmol/L Tris-盐酸、0.5 mol/L磷酸钾(pH6.0)、25 mmol/L Tris-盐酸冲洗,分别平衡3个CV;用150 mmol/L醋酸(pH2.8)洗脱4个CV;用0.1 mol/L NaOH冲洗柱床再生,保留时间15 min;用4个CV的25 mmol/L Tris-盐酸冲洗柱床再平衡。
1.3
低pH病毒灭活条件的确定
将亲和层析收集液分别在pH3.4、3.5、3.6条件下孵育30、60、90 min,检测SEC-HPLC纯度、nrCE-SDS纯度、icIEF酸性峰含量、时间分辨荧光共振能量转移(time-resolved fluorescence resonance energy transfer,TR-FRET)活性等指标,考察对R抗体质量的影响,确定低pH病毒灭活工艺。
1.4
阴离子交换层析工艺开发
以Sepharose Q FF为阴离子交换层析填料,纯化低pH灭活后的R抗体,测定DBC,比较2种平衡液(20 mmol/L 磷酸缓冲液 pH7.0和50 mmol/L Tris-醋酸pH7.5),首先考察蛋白的稳定性,其次考察纯化效果(工艺相关杂质水平)。
1.4.1 样品稳定性比较 用1 mol/L Tris溶液将样品(浓度12.57 mg/mL)pH分别调至与2种平衡液相同,置于室温(25 ℃),将未调pH(pH5.5)样品置于相同条件下作为对照,分别在第1、4、8天考察SEC-HPLC单体、聚体和降解物,nrCE-SDS纯度,icIEF主峰和酸性峰。
1.4.2 纯化效果 按照表2程序进行样品纯化,比较2种缓冲液纯化后样品的收率和工艺相关杂质(HCP、蛋白质A、DNA)水平。

1.4.3 填料DBC的测定 在温度23.2 ℃、浓度4.64 mg/mL样品中加1 mol/L Tris溶液和纯化水调至pH7.5,电导率2.94 mS/cm,用50 mmol/L Tris-醋酸1 mL/min平衡1个CV;1 mL/min上样;用1.0 mol/L NaCl 1 mL/min冲洗3个CV再生;用0.5 mol/L NaCl 1 mL/min冲洗3个CV清洗,完成纯化。过程中取样检测工艺相关杂质去除情况,确定DBC。
1.5
阳离子交换层析工艺开发
使用SP HP填料以线性洗脱方式纯化阴离子层析收集的R抗体。根据平台化经验和产品说明书选用缓冲液A(10 mmol/L柠檬酸,pH5.5)和缓冲液B(10 mmol/L柠檬酸、1 mol/L NaCl,pH5.5),洗脱参数:100%缓冲液A—100%缓冲液B,20 CV;保留时间:4.7 min;进样量:21.9 mg/mL填料。分别收集洗脱峰,检测单体、聚体、降解片段和纯度,考察电荷异质性、HCP、DNA、蛋白质A等,分析产品质量及收率。
1.6
除病毒过滤工艺开发
阳离子纯化收集液蛋白浓度为10.94 mg/mL,使用3款除病毒滤器(每款滤器前对应1款预过滤器)分别进行过滤。设定工艺时长3 h,考察:工艺时间内处理量、通量、流量衰减(与初始滤速相比)等,选择最优的过滤器。
1.7
浓缩/透析和除菌
通过参考膜包说明书、公司平台工艺,确定进液流速为5~6 L/(min·m2),跨膜压力为(0.8±0.3)×105 Pa,其中入口压力(1.2±0.3)×105 Pa,回流端压力(0.5±0.3)×105 Pa。按照确定的参数先浓缩抗体至(40.00±5.00) mg/mL,再以等体积置换方式用10倍料液体积置换成原液缓冲液,最后经0.2 μm膜除菌过滤,获得R抗体原液。
2
结果
2.1
亲和层析
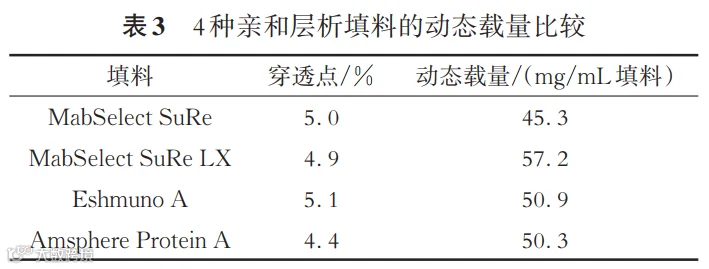
2.1.1 DBC 由表3可见,亲和层析填料MabSelect SuRe LX的DBC最高(57.2 mg/mL填料),其次为Eshmuno A和Amsphere Protein A,MabSelect SuRe的DBC最低。
2.1.2 纯化效果 由表4可见,4种填料纯化收率(低pH灭活前)从高到低顺序为:Amsphere Protein A>MabSelect SuRe LX >Eshmuno A>MabSelect SuRe。
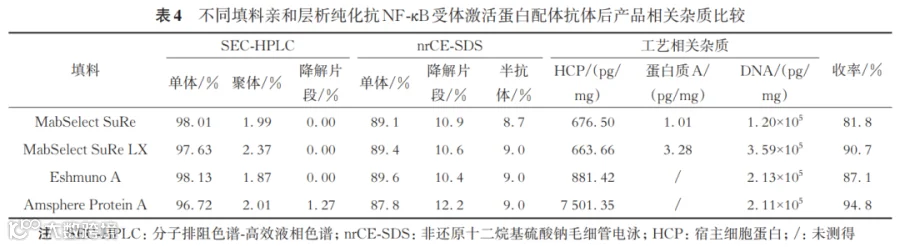
4种填料纯化后的样品,SEC-HPLC单体含量均在96%以上,nrCE-SDS纯度均在87%以上,纯化效果无明显差异;Amsphere Protein A的HCP残留最高,其他3种填料无明显差异;DNA残留无明显差异,MabSelect SuRe LX和MabSelect SuRe的蛋白质A残留无明显差异。
综合分析,4种填料的纯化效果无明显差异,收率范围都可以接受,而MabSelect SuRe填料采购价格明显更低,即具有性价比优势,最终选择MabSelect SuRe作为本品亲和层析填料。
2.2
低pH病毒灭活
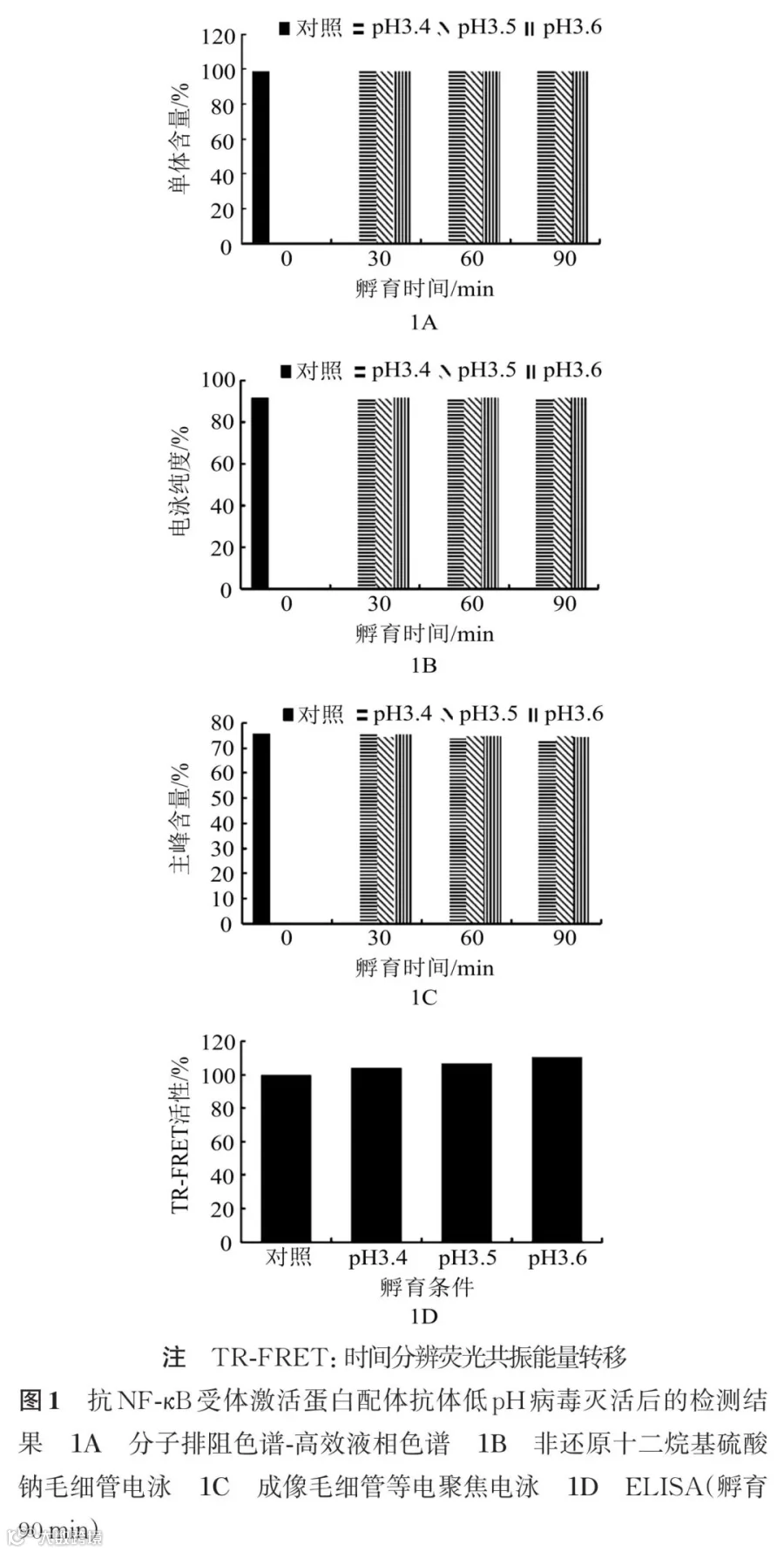
图1的结果显示,pH3.4~3.6条件下,在90 min之内,SEC-HPLC单体含量均在98.5%~100.0%(聚体小于1.5%),nrCE-SDS纯度均在91.3%~92.0%(片段在8.0%~8.7%),icIEF主峰含量均在73%~76%,TR-FRET活性(ELISA)均在105%~112%,无明显差异,即pH3.4~3.6均可作为病毒灭活条件。
2.3
阴离子交换层析
2.3.1 不同缓冲液中样品稳定性 从SEC-HPLC结果(图2)可知:pH值的增加对聚体形成影响不大,pH7.0和pH7.5条件下稳定性优于pH5.5;从nrCE-SDS检测结果(图3)可知:在3种pH条件下R抗体降解差别不大;从icIEF检测结果(图4)可知:放置4.8 d,pH值升高时酸性峰比例虽略有增加,但pH7.0和pH7.5之间无明显差异。
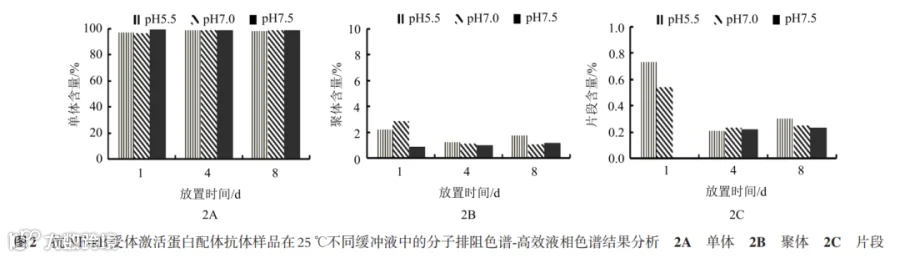
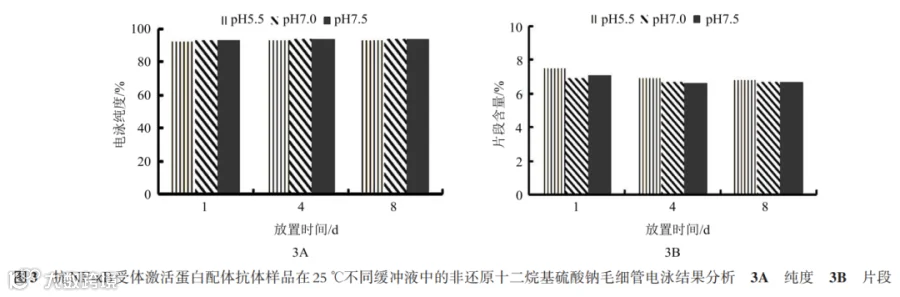
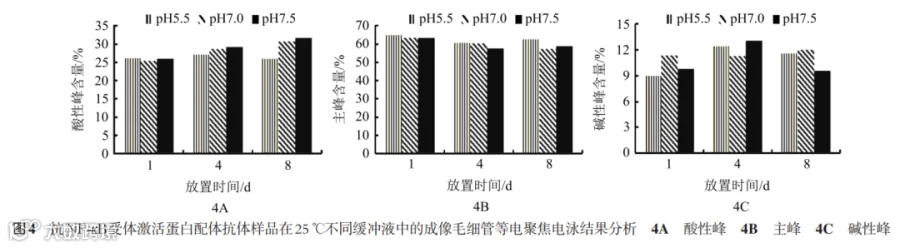
综上,R抗体在20 mmol/L 磷酸缓冲液和50 mmol/L Tris-醋酸缓冲液中稳定性无明显差异。
2.3.2 纯化效果
2.3.2.1 收率 实验1和2的收率分别为93.86%、93.53%,二者无明显差异。
2.3.2.2 工艺相关杂质残留水平 在pH7.5条件下,工艺相关杂质HCP、蛋白质A、DNA残留纯化后与纯化前之比(分别为4.3×10-3、0.065、2.93×10-4)均低于pH7.0条件下(分别为6.4×10-3、0.208、3.69×10-4)。
2.3.3 DBC 综合稳定性和纯化效果,选用50 mmol/L Tris-醋酸作为R抗体项目阴离子交换层析步骤平衡液。因蛋白质A含量较低且在合格范围内,所以不再检测蛋白质A残留。由表5可见,DBC超过69 mg/mL填料后,DNA、HCP残留量开始显著增加,以69 mg/mL填料为该步骤最大上样DBC,为留出安全空间(系数1.15),确定阴离子交换层析最大上样量为60 mg/mL填料。

2.4
阳离子交换层析
如图5所示,根据洗脱峰形将其分为3个组分(从前向后: SP HP 1-1、SP HP 1-2、SP HP 1-3)收集,分别进行检测分析。
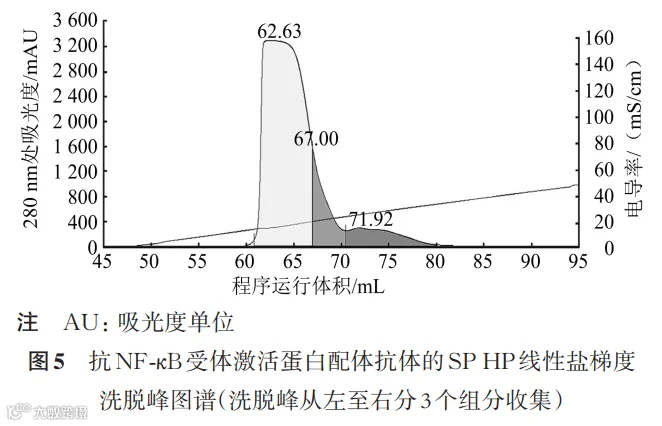
由表6可见,SEC-HPLC结果显示,SP HP纯化后聚体减少;聚体和片段都主要分布在洗脱峰末尾;NR CE-SDS检测发现,线性洗脱的3个组分中都有降解(大小为完整抗体的一半),比例依次增加,表明峰尾有较多半抗体。
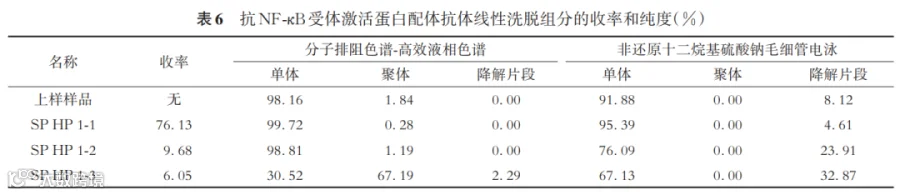
羧肽酶B酶切前后,主要组分SP HP 1-1的主峰比例高于Prolia;洗脱峰尾的酸、碱性峰比例高,见表7。

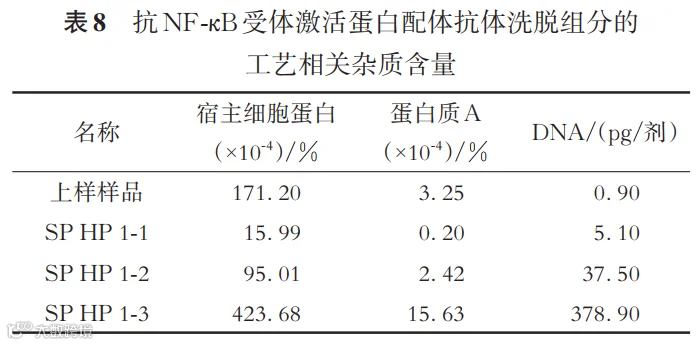
工艺相关杂质方面,SP HP纯化后,主峰HCP、蛋白质A都减少,洗脱峰尾HCP、蛋白质A、DNA杂质都较多,见表8。
综上,高分辨率阳离子填料SP HP可用于R抗体的精纯,通过线性盐梯度洗脱和分段切峰收集,可有效去除产品相关杂质(聚体、片段和碱性峰)和工艺相关杂质(HCP、蛋白质A、DNA),最终工艺收集SP HP 1-1段较纯组分收率可达76%。
2.5
除病毒过滤器选型
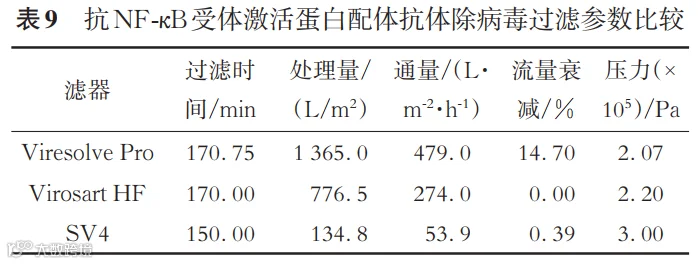
实际工艺时间约为170 min,由表9可见,在该工艺时间内,Viresolve Pro处理量最大,Virosart HF和SV4的分别为其56.88%和12.33%;Viresolve Pro通量也最大,Virosart HF和SV4的分别为其57.20%和11.25%;Viresolve Pro流量衰减相对较快(14.70%),SV4和Virosart HF基本没有衰减。综合上述技术指标和成本,最终选择Millipore公司的Viresolve Pro作为R抗体项目除病毒过滤器。
2.6
超滤、透析及除菌过滤后原液的结果
按照确定的参数执行工艺操作,在中试规模下,获得了纯度和杂质含量符合企业预定标准的R抗体原液,各项结果见表10。

3
讨论
本研究成功开发了抗RANKL单抗的纯化工艺,涵盖从细胞培养液澄清到最终抗体原液制备的全过程。通过系统优化各工艺步骤,包括亲和层析、低pH病毒灭活、离子交换层析、除病毒过滤和超滤透析等,最终获得了高纯度、高收率且符合质量要求的抗体原液。以下对各工艺步骤的开发结果进行讨论。
亲和层析作为单抗纯化的核心步骤,其填料的DBC和纯化效果直接影响最终产品的质量和收率。蛋白质A亲和层析虽以高选择性和载量成为抗体捕获的首选方法,但其成本较高且可能引入配基脱落等问题。本研究比较了4种蛋白质A亲和层析填料(MabSelect SuRe、MabSelect SuRe LX、Eshmuno A和Amsphere Protein A)的性能。结果表明,MabSelect SuRe LX虽DBC最高(57.2 mg/mL填料),但其纯化后的HCP残留较高;而MabSelect SuRe虽然DBC较低(45.3 mg/mL填料),但纯化效果更优,HCP和DNA残留较低,且产品相关杂质(如聚体和片段)较少。选择MabSelect SuRe作为亲和层析填料,能够在保证产品质量的同时兼顾工艺的经济性。
低pH病毒灭活是单抗纯化工艺中不可或缺的步骤,主要用于灭活脂包膜病毒。本研究考察了不同pH值(3.4~3.6)和孵育时间(30~90 min)对R抗体质量的影响,SEC-HPLC、icIEF和TR-FRET等检测结果表明,低pH处理后的抗体单体含量、电荷异质性和活性均保持稳定。pH3.5、60 min的灭活条件被确定为最佳工艺参数。
阴离子交换层析主要用于去除工艺相关杂质(如HCP、DNA和蛋白质A残留)。本研究比较了2种平衡液的纯化效果,发现50 mmol/L Tris-醋酸在HCP和DNA去除方面表现更优。DBC结果表明,50 mmol/L Tris-醋酸的最大上样载量为60 mg/mL填料,能够有效控制杂质残留。选择50 mmo/L Tris-醋酸作为阴离子交换层析的平衡液,能够在不影响收率的前提下,显著提高纯化效果。
阳离子交换层析作为精纯步骤,主要用于去除产品相关杂质(如聚体、片段和电荷异质体)以及残留的工艺相关杂质。本研究采用SP HP填料进行线性盐梯度洗脱,结果显示,通过分段收集洗脱峰,能够有效去除聚体和酸性峰,同时显著降低HCP和DNA残留。主峰组分的收率达到76%以上,且单体含量高达99.7%,表明SP HP填料在R抗体精纯中具有优异的性能。
除病毒过滤是确保抗体药物安全性的关键步骤。本研究比较了Millipore Viresolve Pro、Sartorius Virosart HF和Pall SV4这3款滤器的性能。结果显示,Viresolve Pro在处理量、通量和流量衰减方面表现最优,能够在170 min内完成1 365 L/m²的过滤量。选择Viresolve Pro作为除病毒过滤器,能够满足大规模生产的需要。
超滤透析用于将抗体浓缩至目标浓度并完成缓冲液置换。本研究参考平台工艺,确定了进液流速5~6 L/(min·m2)和跨膜压力(0.8±0.3)×105 Pa等关键参数。使用Millipore PLCTK 30 kDa超滤膜包,成功将抗体浓缩至(40.00±5.00) mg/mL,并以等体积置换方式完成缓冲液置换,再经过除菌过滤获得原液。
尽管本研究成功开发了抗RANKL单抗的纯化工艺,但在实际生产中仍需进一步优化,如可以探索新型亲和层析填料或混合模式层析技术,以进一步提高纯化效率和产品质量。随着连续生产工艺的发展,未来可以考虑将部分步骤整合为连续操作,以进一步提高生产效率和降低成本。总之,本研究为抗RANKL单抗的纯化工艺开发提供了系统的技术路线和实验依据,为抗体药物的开发提供了参考。
作者
冉永梅1,2 赵永强2 许方岩2 郭春1
1沈阳药科大学制药工程学院,沈阳 110016;2珠海市丽珠单抗生物技术有限公司研发部,珠海 519045
通信作者:
郭春,Email:chunguo@syphu.edu.cn
赵永强,Email:yq_008008@126.com
引用本文:冉永梅, 赵永强, 许方岩, 等. 抗RANKL单克隆抗体纯化工艺的开发 [J]. 国际生物制品学杂志, 2025, 48(5): 301-308.
DOI: 10.3760/cma.j.cn311962-20250211-00011

《国际生物制品学杂志》为中华医学会系列杂志,创刊于1978年10月,目前由中华人民共和国国家卫生健康委员会主管、中华医学会和上海生物制品研究所有限责任公司主办。现任主编李秀玲,编委团队共50人,审稿专家116人。
本刊重点介绍国内外生物制品学领域的新进展、新动态、新技术和新成就,设有述评、综述、论著、短篇论著、病例报告、学习交流、国际会议介绍等栏目。
投稿流程
方法一:登录中华医学会杂志社学术期刊出版服务平台 https://medpress.yiigle.com,选择《国际生物制品学杂志》进行投稿。
方法二:登录《国际生物制品学杂志》官网:http://www.ijbiol.com,点击投稿系统入口进行投稿。
投稿详情请致电编辑部郭老师18616609021或021-62834337。
邮件订阅

点击官网右下角Email Alert订阅本刊,可免费获取当期目录及文章电子版!
分享、在看、点赞,请至少给我们一个哦




